توضیحات
| ml | 0/5×1 | Ser | Control | ml | 0/5×1 | 0 | FPSA | CAL |
| ml | 6×1 | Conj | Enzyme | ml | 0/5×1 | 0/3 | FPSA | CAL |
| ml | 6×1 | Subs | Chrom | ml | 0/5×1 | 1 | FPSA | CAL |
| ml | 6×1 | Solu | Stop | ml | 0/5×1 | 2 | FPSA | CAL |
| ml | 25×1 | 20X | Wash Buf | ml | 0/5×1 | 5 | FPSA | CAL |
| ºC | 8 – 2 | 48Test |
Microplate |
ml | 0/5×1 | 10 | FPSA | CAL |
| Free PSA Elisa 48 Test |
||||||||
کیت الایزا برای تعیین غلظت آنتی ژن آزاد اختصاصی پروستات
Human Free Prostate Specific Antigen (FPSA) ELISA Kit
مقدمه :
آنتی ژن اختصاصی پروستات (PSA) یک گلیکوپروتئینی است که عمدتا توسط سلول های اپیتلیوم غده پروستات تولید می شود. غلظت آن در خون طی بیماری های پروستات شامل سرطان پروستات، بزرگ شدن خوش خیم غده پروستات و عفونت پروستات افزایش مییابد و نشانگر خوبی جهت تشخیص و پیگیری درمان بیماری های پروستات می باشد. ملکول PSA در خون بدو شکل آزاد و پیوند به پروتئین های سرم وجود دارد که براساس نوع بیماری نسبت این دو تغییر می کند که این نسبت بیانگر خوبی از نوع بیماری غده پروستات می باشد.
اساس روش اندازه گیری :
کیت الایزای FPSA موجود، براساس سنجش ایمونولوژیکی آنزیمی ساندویچی تهیه شده است. PSA موجود درنمونه ها بعنوان آنتی ژن به دو آنتی بادی زوج اختصاصی خود متصل می گردد. هر دو آنتی بادی از نوع منوکلونال موشی هستند که یکی برروی فاز جامد (چاهک ها) پوشش داده شده است و دیگری به آنزیم HRP متصل شده است. نمونه مورد آزمایش که دارای FPSA است، در معرض دو آنتی بادی قرار می گیرد. پس از زمان انکوباسیون، چاهک ها تخلیه شده و شستشو داده می شوند تا آنتی بادی متصل به آنزیم HRP اضافی خارج گردد. سپس به هرچاهک سوبسترای آنزیم اضافه می شود که فعالیت آنزیم بطور مستقیم با غلظت FPSA در نمونه ها متناسب است. استانداردهای FPSA با غلظت مشخص، همراه با نمونه های مجهول آزمایش می شوند که براساس منحنی استاندارد جذب نور در مقابل غلظت FPSA، غلظت نمونه های مجهول بدست می آید.
معرف ها :
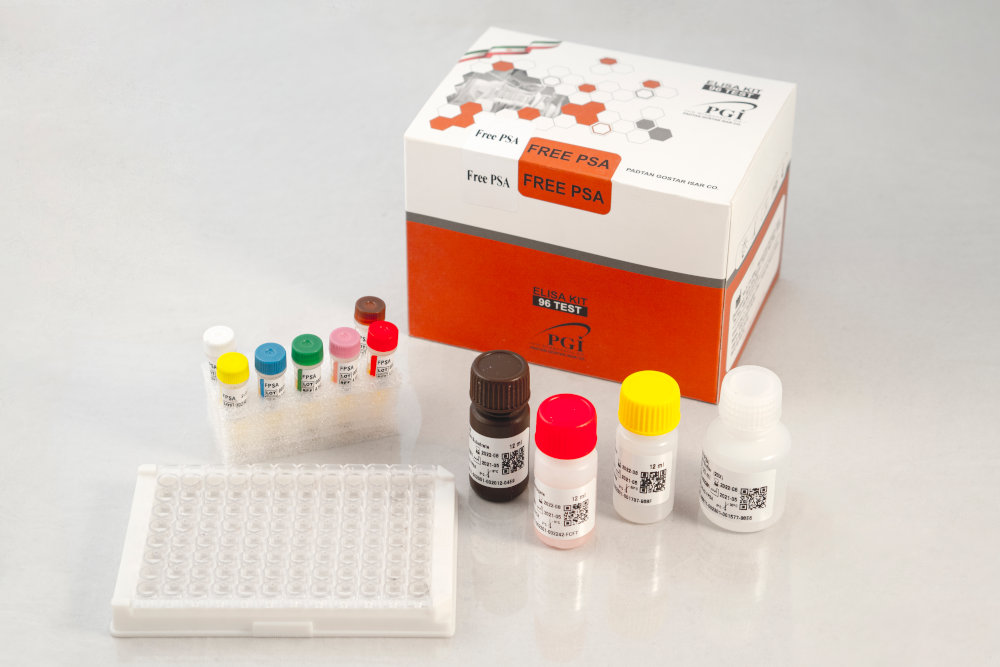
1- میکروپلیت پوشش داده شده: شامل 96 چاهک جداشدنی که با آنتی بادی منوکلونال موشی Anti-FPSA پوشش داده شده اند.
2- کونژوگه آنزیمی (HRP-Anti-PSA) : یک ویال 12 میلی لیتری آماده مصرف.
3- استانداردها : 6 ویال یک میلی لیتری از استاندارد FPSA با غلظت های 0، 3/0، 1، 2، 5 و 10 نانوگرم در میلی لیتر (ng/ml) که در سرم نرمال انسانی تهیه شده و از تیومرسال بعنوان نگهدارنده استفاده شده است.
4- سرم کنترل: یک ویال یک میلی لیتری آماده مصرف.
5- محلول شستشو دهنده غلیظ (20X) : یک ویال 25 میلی لیتری محلول شستشو که برای تهیه محلول شستشوی آماده مصرف لازم است این محلول به نسبت 20/1 با آب دیونیزه رقیق شود.
6- محلول رنگ زا: یک ویال 12 میلی لیتری محلول آماده مصرف
7- محلول متوقف کننده واکنش: یک ویال 12 میلی لیتری اسیدسولفوریک یک نرمال.
مواد و وسایل مورد نیاز که در کیت موجود نیست :
1- سمپلر 50 -100 µl
2- آب دیونیزه
3- دستگاه الایزا ریدر دارای فیلتر 450 نانومتری و در صورت امکان 630 نانومتری بعنوان فیلتر رفرانس.
4- انکوباتور 1 ± 37 درجه سانتی گراد
5- کاغذ جاذب رطوبت
نکات قابل توجه برای مصرف کنندگان :
1- از تماس محلول متوقف کننده واکنش (1N H2SO4) با پوست خودداری کنید. در صورت تماس، با آب فراوان آنرا بشوئید.
2- از استفاده از مواد پس از تاریخ انقضاء خودداری کنید و از مخلوط کردن یا استفاده از کیت ها با شماره بچ مختلف پرهیز نمائید.
3- درب ظروف را پس از استفاده ببندید و از تعویض درب ها جدا خودداری کنید.
4- محلول های محتوی مواد افزودنی یا نگهدارنده مثل سدیم آزاید نباید در واکنش آنزیمی وارد شوند.
5- کیت های باز نشده پس از تحویل باید در دمای 8-2 درجه سانتی گراد (یخچال) نگه داری شوند. میکروپلیت باید در کیسه در بسته به همراه ماده جاذب رطوبت نگه داری شود. کیت باید تا تاریخ انقضا استفاده شود (یکسال از زمان تولید). برای اطلاع از تاریخ انقضا به برچسب کیت مراجعه شود.
6- کیت های باز شده حداقل به مدت 4 ماه پایدار خواهد ماند، اگر در شرایط توصیه شده در بالا نگهداری شود.
7- توصیه می شود که بیشتر از 32 چاهک در هر مرحله کاری استفاده نشود. اگر پی پت به صورت دستی انجام می گیرد، پی پت کردن همه استانداردها، نمونه ها ، کنترل ها باید در 5 دقیقه تمام شود. برای پی پت کردن کل پلیت 96 تستی باید از پی پت اتوماتیک استفاده شود.
8- فرایند شستشو خیلی مهم است. شستشوی ناکافی باعث کاهش دقت و افزایش کاذب جذب می شود.
تهیه و جمع آوری نمونه :
1- آزمایش را باید بر روی نمونه های سرمی انجام داد. نمونه های شدیدا همولیزه و دارای چربی باید حذف شوند.
2- نمونه ها را می توان برای 24 ساعت1 در دمای 2 تا 8 درجه سانتیگراد و برای زمان های طولانی تر (تا سی روز) در دمای 20- درجه سانتیگراد نگهداری نمود.
3- از انجماد و ذوب مکرر نمونه ها باید خوداری کرد.
آماده سازی معرف ها :
1- کلیه معرف ها را به دمای اتاق برسانید. قبل از استفاده آنها را به آرامی کاملا سر و ته نمائید.
2- برای تهیه محلول شستشوی آماده مصرف، یک حجم از بافر شستشو غلیظ (20X) را با 19 حجم آب مقطر رقیق نمائید. محلول شستشو در دمای اتاق به مدت 2 ماه پایدار است .
روش انجام آزمایش :
1- تعداد چاهک های کوت شده برای استانداردها، سرم کنترل و نمونه های بیمار را بصورت 2 تایی انتخاب کنید و مابقی چاهک ها را همراه ماده آبگیر درون کیسه مخصوص قرار داده و درب آنرا ببندید.
2- lµ 50 از استانداردها، سرم کنترل و نمونه ها به چاهک مورد نظر اضافه کنید.
3- lµ 100 از کونژوگه آنزیمی به تمام چاهک ها اضافه کنید.
4- پلیت را بمدت 30 ثانیه به آرامی تکان دهید تا محتویات چاهک ها خوب مخلوط شوند (در این مرحله مخلوط کردن کامل بسیار مهم است). سپس درب چاهک ها را با برچسب مخصوص پوشانده و پلیت را بمدت یک ساعت در درجه حرارت 37 درجه سانتیگراد انکوبه کنید.
5- محتویات چاهک ها را خالی کرده و چاهک ها را 5 بار با 300 میکرولیتر بافر شستشوی آماده مصرف بشوئید. برای شستشوی چاهک ها، ابتدا 300 میکرولیتر بافر شستشو را داخل چاهک بریزید، سپس چاهک ها را وارونه کرده و همراه با تکان دادن خالی کنید و در انتهای شستشو، با ضربات ملایم بر روی کاغذ جاذب تمامی مایع موجود در چاهک ها را تخلیه نمائید.
6- 100 میکرولیتر از سوبسترای آماده مصرف به تمامی چاهک ها اضافه کنید و آنها را بمدت 20 دقیقه بدون تکان دادن، در دمای اتاق و تاریکی انکوبه نمائید.
7- 100 میکرولیتر از محلول متوقف کننده واکنش به همه چاهک ها اضافه کنید. مدت 15 ثانیه مخلوط شود .خیلی مهم است تا مطمئن شوید رنگ آبی کاملاً به رنگ زرد تغییر پیدا کرده است. سپس جذب نور هر چاهک را در طول موج 450 نانومتر با دستگاه الایزا ریدر قرائت نمائید (در صورت امکان از طول 630 نانومتر بعنوان فیلتر رفرانس استفاده کنید). سنجش جذب نوری باید حداکثر تا 30 دقیقه پس از اتمام آزمایش انجام شود.
محاسبه نتایج
1- با استفاده از میانگین جذب نوری استانداردها (محور Y) و غلظت مشخص آنها (محور X) برروی کاغذ میلی متری، منحنی استانداردی رسم کنید.
2- میانگین جذب نوری برای هر نمونه را بدست آورده و روی محور Y جای آنرا پیدا کنید. سپس نقطه مذکور را توسط خطی به منحنی وصل کنید. از نقطه بدست آمده خطی عمود بر محور X وارد کنید تا نقطه تلاقی که نشان دهنده غلظت نمونه است، بدست آید.
3- با استفاده از کامپیوتر این محاسبات ساده خواهد شد.
راهنمای محاسبه
مقادیر جذب نوری ارائه شده در جدول ذیل تنها بعنوان راهنمایی آورده شده است و هر آزمایشگاهی باید برای هر بار آزمایش یک منحنی استاندارد جدید بدست آورد.
| OD | FPSA Con. (ng/ml) | No. |
| 0.02 | 0 | 1 |
| 0.13 | 0.3 | 2 |
| 0.31 | 1 | 3 |
| 0.59 | 2 | 4 |
| 1.7 | 5 | 5 |
| 2.8 | 10 | 6 |
مقادیر طبیعی
1- هر آزمایشگاه باید دامنه طبیعی را برای خود به دست آورد. این مقادیر فقط برای راهنمایی داده شده است.
| مردان طبیعی | کمتر یا مساوی 3/1 نانوگرم در میلی لیتر |
2- اندازه گیری غلظت Free PSA حتما باید با اندازه گیری غلظت Total PSA همراه باشد تا نسبت FPSA به TPSA برای تفسیر نتایج بدست آید.
3- معمولا در حالت سرطانی نسبت FPSA به TPSA کاهش می یابد. نسبت FPSA به TPSA حدود 25 درصد معمولا احتمال هیپرپلازی خوش خیم پروستات را نشان می دهد. اغلب مردان با سرطان پروستات یک نسبت کمتر از 15 درصد را نشان می دهند. براساس نظر American Cancer Society و National Cancer Institute برای نسبت کمتر از 7 درصد، فرد باید تحت بیوپسی قرار گیرد.
خصوصیات کیت:
1- حساسیت آنالیتیکال (حد تشخیص) : برای تعیین حد تشخیص 20 مرتبه استاندارد صفر آزمایش شد. حد تشخیص از 2 انحراف معیار (SD) بالاتر از میانگین جذب در غلظت صفر بدست آمد. حد تشخیص برای این کیت ng/ml 0.05 بدست آمد.
2- ویژگی: واکنش متقاطع آنتی بادی های مونوکلونال مورد استفاده در این آزمایش برای سایر پروتئین ها بسیار پائین بدست آمد.
3- دقت : برای محاسبه میزان دقت در یک روز و روزهای مختلف، آزمایش بر روی 3 نمونه سرم 15 بار تکرار شد که ضریب تغییرات به شرح ذیل است.
ضریب تغییرات در روز
| نمونه سرم | دفعات تکرار | میانگین (ng/ml) | انحراف معیار | ضریب تغییرات (CV) |
| 1 | 15 | 0.8 | 0.05 | 6.5 |
| 2 | 15 | 4.3 | 0.21 | 5.05 |
| 3 | 15 | 8.2 | 0.26 | 3.2 |
ضریب تغییرات در روزهای مختلف
| نمونه سرم | دفعات تکرار | میانگین (ng/ml) | انحراف معیار | ضریب تغییرات (CV) |
| 1 | 15 | 1.2 | 0.07 | 6.8 |
| 2 | 15 | 3.8 | 0.21 | 5.39 |
| 3 | 15 | 8.9 | 0.25 | 2.8 |
4- خطی بودن : سه نمونه مختلف سرمی با استاندارد صفر به نسبت های 1:2، 1:4 و 1:8 رقیق شدند. سپس غلظت FPSA در آنها با استفاده از کیت محاسبه شد که نتایج ذیل بدست آمد.
| نمونه سرمی | غلظت اولیه (ng/ml) | درصد بازیابی | ||
| 1:2 | 1:4 | 1:8 | ||
| 1 | 4.7 | 108 | 110 | 110 |
| 2 | 6.8 | 106 | 104 | 106 |
| 3 | 9.8 | 96 | 104 | 109 |
5- اثر هوک : اثر هوک تا غلظت ng/ml200 ظاهر نمی شود.
محدودیت ها:
نتایج قابل قبول و تکرارپذیر زمانی حاصل خواهد شد که روش کار با درک کامل دستورالعمل موجود در کیت و مهارت های عملی خوب انجام گیرد.
کنترل کیفی:
عملکرد آزمایشگاهی خوب مستلزم این است که در هر سری کاری همراه با هر منحنی استاندارد نمونه های کنترل کیفی نیز برای تایید شاخص های اجرایی سنجش، آنالیز شوند. برای تضمین شاخص های اجرایی صحیح و برای تعیین مقادیر میانگین و دامنه های قابل قبول تعداد نمونه های کنترلی که آنالیز می شوند باید از لحاظ آماری معنی دار باشند.
برای دانلود PDF بروشور اینجا کلیک کنید
نقد و بررسیها
هیچ دیدگاهی برای این محصول نوشته نشده است.